질병관리본부 국립보건연구원과 셀트리온은 13일 코로나19 바이러스 항체치료제 개발을 위해 실시한 중화능력 검증에서 최종 항체 후보군 38개를 확보했다고 밝혔다.
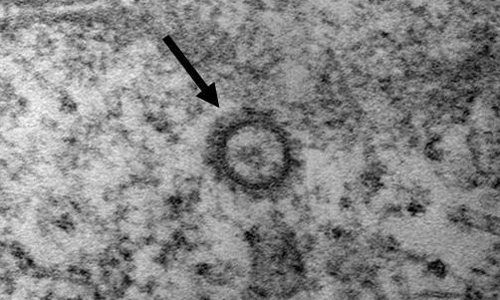
질본과 셀트리온은 지난 2일부터 협업을 시작해 1차 코로나19 항체 후보군 300개 중 항원과의 결합력이 높은 106개 항체를 대상으로 1, 2차에 거쳐 바이러스를 무력화하는 중화능력을 검증해 38개를 추렸다고 설명했다. 이 중 14개의 항체는 강력한 중화능력을 보이는 것으로 알려졌다.
중화능력은 항체와 바이러스를 혼합해 숙주 세포에 감염시킨 후 항체에 의해 숙주세포가 살아나는 정도를 알아보는 방식으로 검증한다.
셀트리온은 최종 항체 후보군을 대상으로 세포주 개발 단계로 돌입한다. 세포주 개발이 완료되면 인체임상물질 대량생산에 착수하는 동시에, 질본에서 실험쥐 대상 효력시험 및 영장류 대상 독성시험을 병행해 개발 기간을 최대한 앞당긴다는 방침이다. 7월 중 인체 임상시험 돌입을 목표로 하고 있다.
식품의약품안전처도 이날 신속한 코로나19 치료제 및 백신 개발을 위해 품목별 전담관리자를 지정해 맞춤 지원하고, 임상시험 심사 및 허가 기간을 대폭 단축하는 내용을 담은 ‘고강도 신속 제품화 촉진 프로그램’(고(GO)·신속 프로그램)을 가동한다고 밝혔다.
우선 연구소 등에서 후보물질 탐색 시 제품 상용화 가능성이 있는 물질을 결정하는 데 과학적 자문을 제공한다. 기존에 사용 중인 의약품의 코로나19 치료 효과를 확인하기 위한 ‘약물 재창출’ 관련 임상시험은 늦어도 7일 이내에 심사를 완료할 계획이다.
통상 30일가량 소요되는 임상시험 심사 기간도 대폭 줄인다. 사용 경험이 있는 물질의 경우 7일 이내로, 신물질의 경우 15일 이내로 임상시험 심사 기간을 단축하기로 했다. 이 밖에 의약품 규제기관 국제 연합(ICMRA) 등 국제적 공조를 통해 각국에서 진행되는 임상시험 및 심사정보를 공유할 예정이다.
남혜정 기자 hjnam@segye.com
[ⓒ 세계일보 & Segye.com, 무단전재 및 재배포 금지]
![[설왕설래] ‘악의 축’ 부활](http://img.segye.com/content/image/2024/04/28/128/20240428510563.jpg
)
![[특파원리포트] 숨겨진 총](http://img.segye.com/content/image/2023/07/16/128/20230716516186.jpg
)
![[구정우칼럼] 양극화를 치유할 기회의 창](http://img.segye.com/content/image/2023/02/26/128/20230226514242.jpg
)
![[심호섭의전쟁이야기] 무대 뒤편으로 은퇴한 ‘역전의 상륙작전’](http://img.segye.com/content/image/2024/02/18/128/20240218510386.jpg
)








